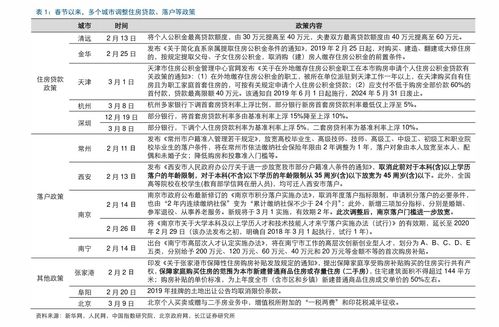
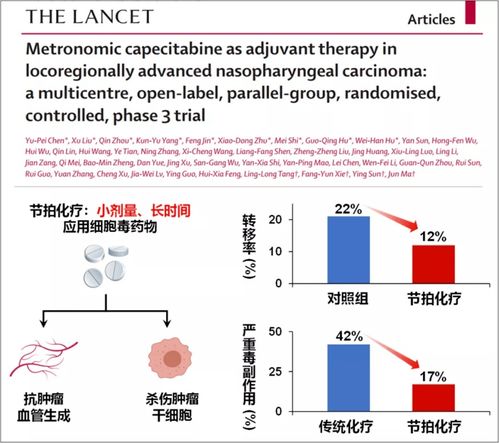
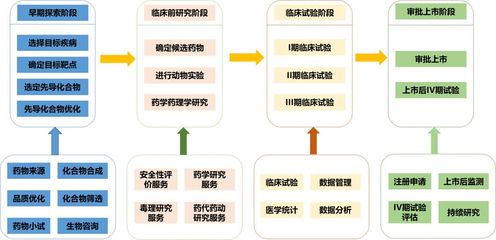
2020年代謝性疾病基礎研究與轉化醫學研究進展盤點
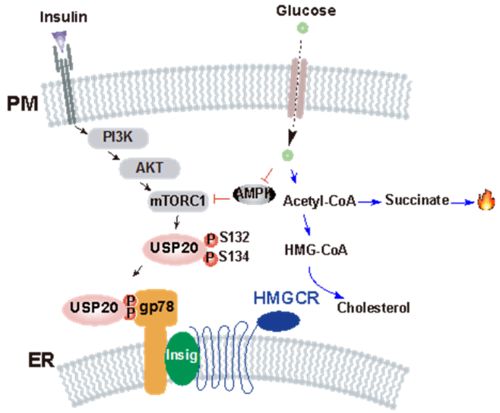
進入2020年代,全球代謝性疾病(如2型糖尿病、非酒精性脂肪性肝病、肥胖癥等)的發病率持續攀升,已成為威脅人類健康的重大公共衛生問題。與此相應,醫學界在代謝性疾病的基礎研究與轉化醫學領域也取得了顯著進展,為疾病的預防、診斷和治療帶來了新的希望。本文將對2020年以來的關鍵性進展進行梳理與盤點。
一、基礎研究深度拓展:機制解析邁向系統化與精細化
- 腸道微生物組與代謝穩態:研究進一步證實,腸道菌群及其代謝產物(如短鏈脂肪酸、膽汁酸、支鏈氨基酸等)在宿主能量代謝、胰島素敏感性和炎癥調節中扮演核心角色。通過宏基因組學、代謝組學等多組學技術,科學家們正在繪制更精細的“腸-肝軸”、“腸-腦軸”在代謝疾病中的調控網絡,并識別出關鍵的功能菌株和代謝通路。
- 免疫代謝與慢性炎癥:代謝性疾病被視為一種慢性低度炎癥狀態。研究深入揭示了固有免疫和適應性免疫細胞(如巨噬細胞、T細胞)在脂肪組織、肝臟和胰腺等代謝器官中的功能可塑性及其與營養信號、代謝底物的相互作用,為靶向免疫代謝治療提供了新思路。
- 細胞器互作與代謝調控:細胞器間的動態接觸與通信(如線粒體-內質網互作、脂滴與其他細胞器的互作)對維持細胞代謝平衡至關重要。這些互作失調被證實與胰島素抵抗、脂質堆積等病理過程密切相關,成為基礎研究的新前沿。
- 表觀遺傳與代謝記憶:環境因素(如營養過剩)通過表觀遺傳修飾(DNA甲基化、組蛋白修飾、非編碼RNA)影響基因表達,且這種影響可能具有持久性甚至可遺傳性。這解釋了早期生活經歷對成年后代謝疾病風險的深遠影響,并為干預提供了潛在靶點。
二、轉化醫學成果豐碩:從實驗室到臨床的橋梁日益穩固
- 新型治療靶點與藥物開發:基于基礎研究發現,多個新靶點藥物進入臨床研究階段。例如,針對胰高血糖素樣肽-1(GLP-1)、葡萄糖依賴性促胰島素多肽(GIP)和胰高血糖素受體的多重激動劑(如Tirzepatide)在降糖、減重方面展現出超越傳統藥物的卓越療效,已獲批上市。針對肝臟脂肪合成的乙酰輔酶A羧化酶(ACC)抑制劑、甲狀腺激素受體β(THR-β)激動劑等在治療非酒精性脂肪性肝炎(NASH)的臨床試驗中也取得積極結果。
- 數字健康與智能監測:可穿戴設備、連續血糖監測(CGM)系統、人工智能輔助診斷模型的廣泛應用,實現了對代謝參數的實時、動態、個性化監測與管理。這不僅能優化治療方案,也為早期預警和生活方式干預提供了強大工具。
- 細胞治療與基因治療的探索:盡管仍處早期階段,但利用干細胞衍生胰島細胞治療糖尿病、利用基因編輯技術糾正致病基因突變等前沿方向正從概念走向實踐,為根治某些代謝性疾病帶來了曙光。
- 精準營養與個性化干預:基于個體基因組、微生物組、代謝組特征的精準營養建議,正逐漸取代“一刀切”的飲食指南。研究表明,個體對同一食物的血糖、血脂反應差異巨大,個性化營養干預能更有效地改善代謝健康。
三、挑戰與未來展望
盡管進展顯著,代謝性疾病研究仍面臨挑戰:疾病的極端異質性要求更精細的分型;從動物模型到人體應用的轉化效率有待提高;長期療效與安全性需要更多數據驗證;醫療可及性與衛生經濟學問題亟待解決。
代謝性疾病的研究將繼續朝著多組學整合、時空動態解析、人工智能深度參與的方向發展。轉化醫學的重點將不僅在于開發新藥,更在于構建整合藥物、設備、數字工具和生活方式干預的全方位、全周期健康管理生態系統。通過基礎研究的不斷深化與轉化路徑的持續優化,人類有望在2030年代迎來代謝性疾病防控的突破性進展。
如若轉載,請注明出處:http://www.jjzdbl.cn/product/83.html
更新時間:2026-04-18 22:07:04